(生物科学专业毕业论文) 糖皮质激素对牛NCOR1基因转录活性调控作用研究
一、选题的目的和意义;
NCoR1作为一个重要的辅抑制子对脂肪细胞分化和肌肉发育有重要作用,使NCoR1作为肥胖病和肌肉萎缩疾病的潜在治疗靶点。同时,NCOR1基因在小鼠上的研究也提示我们该基因可能成为培育产肉量高、肌内脂肪含量高的肉牛新品种的重要候选功能基因。糖皮质激素调控及在成脂分化脂代谢中作用
二、选题的依据;
核受体辅抑制子(Nuclear receptor corepressor 1, NCOR1)属于类固醇激素-视黄酸受体相关辅抑制子家族,经与其它配体结合形成转录复合物,通过介导染色体紧缩、组蛋白乙酰化以及直接互作等多种方式调控基因表达,从而在机体的生长发育、细胞分化等体内许多生理过程中发挥作用(Oberoi et al.2011;Pourcet et al.2010)。近年来研究发现, NCOR1与NCOR2(NCOR1旁系同源)可以特异结合脂肪细胞分化重要调节蛋白PPARγ,并抑制其调控的下游基因转录活性,进而抑制脂肪细胞分化(Yu et al.2005)。脂肪细胞特异性敲除NCOR1基因小鼠(AKO小鼠)中PPARγ相关基因上调,而周期素依赖性激酶5 (Cyclin-dependent kinase-5, CDK5)调节的PPARγ ser-273位磷酸化水平下降,而PPARγ磷酸化水平的下降可能进一步激活下游调控因子,促进脂肪形成,导致小鼠肥胖 (Choi et al.2010; Li et al.2011)。而肌肉组织特异性敲除NCOR1基因,导致小鼠肌肉量以及线粒体数量和活性都有所增加,使得小鼠运动耐力增强。进一步研究发现,NCOR1调节了肌肉增强因子2 (Myocyte enhancer factor-2, MEF2)、雌激素受体相关受体(Estrogen receptor related receptor, ERR)和PPARδ等控制肌肉功能的转录因子活性(Yamamoto et al.2011)
三、国内外研究概况;
1.对糖皮质激素受体及其调控基因转录的研究
糖皮质激素受体(glucocorticoid receptor,GR)在机体的生命活动中具有重要作用。它是激素核受体家族中的一个主要成员,同时也是一种重要的核转录因子,转录调控多种基因表达。糖皮质激素作用的发挥必须与糖皮质激素受体结合。糖皮质激素受体不仅能参与机体应激反应,而且具有抗炎抗免疫作用和促细胞凋亡作用。目前已知的 GR 有三种类型,分别为 α、β 和 P 型,糖皮 质激素受体在应激及 GC 抵抗中扮演着重要的角色。
1.1糖皮质激素受体的结构及其功能区
GR 是可溶性单链多肽组成的磷蛋白,人类的 GR 基因位 于 5 号染色体上,由 9 个外显子组成。GR 基因在第 9 个外显 子处经不同剪接生成两种不同 GR 蛋 白 质 形 式 , 分 别 称 为GRα 和 GRβ。它们的基因结构高度同源,其中前 8 个外显子结构完全相同,第 9个外显子分别为 9α和9β外显子9α和 9β分别构成 GRα 和 GRβ 基因,GRα 和 GRβmRNA 的 N 端的 727 个氨基酸组成完全相同,区别在于 C 端。结构上 由 3 个功能区组成,包括有基因转录激活功能的氨基端、位于中 部 的 DNA 结合区和含有激素结合区的羧基端 。另 外 ,在DNA 结合区和激素结合区之间还有一个 D 区域,与 GR 向核内的移行有关
1.2 糖皮质激素受体的分布与调节
机体所有的有核细胞均表达一定数量的 GRα,GRβ 则 主要分布于 T 淋巴细胞、巨噬细胞和嗜碱性粒细胞。GRα 广泛存在于脑内神经元和神经胶质细胞,但以边缘系统的海马、隔区、下丘脑分泌 CRH 和 AVP 的小细胞神经元、垂体促肾上腺皮质激素分泌细胞最为丰富。脑干的上行单胺能神经元、丘脑 核 团 、纹 状 体 、杏 仁 核和皮质也存在相当丰富的 GRα。RβmRNA 仅存在于下丘脑、海马神经元,且最多处仅为GRα 的 1%。GRαmRNA 表达水平明显高于 GRβmRNA,多 数细胞中 GRαmRNA 与 GRβmRNA 表达量之比大于 500。有些学者认为炎症可使 GRα 亲合力下降以及对激素 治疗的敏感性减退,机制可能与细胞因子的作用有关。但 GRβ的表达和调节与 GRα 相比有不同之处,很多致炎细胞因子可 显著上调 GRβ 的表达。研究结果发现,溃疡性结肠炎患者肠 粘 膜 细 胞 中 GRα 与 GRβ 均有表达,在激素敏感组中 GRα 的表达较抵抗组高,而 GRβ 含量较抵抗组低,这一方面明 GRα 含量越高,疗效越敏感;GRβ 含量越高,疗效越差。
1.3 糖皮质激素受体的作用机制
GR 作用机制相当复杂,可能为多种机制共同作用。GR 是一种配体激活的内源性转录因子。当无 GC 时,GR 在细胞质 内以蛋白复合体形式存在,此复合体由 1 个受体分子,1 分子 亲免素,2 分子热休克蛋白 90 (Hsp90),1 分子 Hsp70 和 1 分子 Hsp56 组成,不具有刺激转录的活性。当 GC 以被动扩散进入 细胞质后,GR 则与 HSP90 等解离并发生自身构象改变,并暴 露出被覆盖的 DNA 结合区,从而启动核转位信号,使 GR-GC 复合物进入细胞核,通过 NDA 结合区与靶基因上的激素结合 区结合,GR-GC 复合物与激素结合区结合后还不能调控靶基 因的转录,尚需与转录共激活因子及基础转录复合物中转录因 子相互作用,才能特异性地促进靶基因的表达而发挥激素效 应。GR 的结合活性由两方面的因素决定:一是 GR 的数量;另 一个是 GR 的配体亲和力,Hsp90 是影响 GR 亲和力的重要因 素之一。在这个机制中,Hsp90 的作用至关重要,只有它与 GR 的配体结合域结合后,GR 才具有对 GC 的高亲和性。如缺 乏 Hsp90 时 GR 对 GC 的亲和力是极低的。合适的 Hsp90/GR 值对于维持 GR 的亲和力和结合活性是非常重要的。
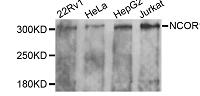
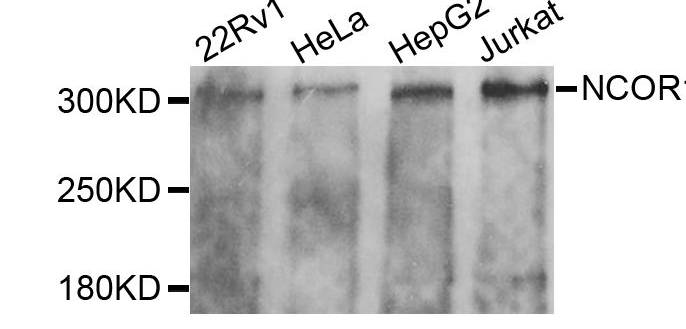
2.对NCOR1基因的研究
核受体辅抑制子(Nuclear receptor corepressor 1, NCOR1)属于类固醇激素-视黄酸受体相关辅抑制子家族,经与其它配体结合形成转录复合物,通过介导染色体紧缩、组蛋白乙酰化以及直接互作等多种方式调控基因表达,从而在机体的生长发育、细胞分化等体内许多生理过程中发挥作用(Oberoi et al.2011;Pourcet et al.2010)。近年来研究发现, NCOR1与NCOR2(NCOR1旁系同源)可以特异结合脂肪细胞分化重要调节蛋白PPARγ,并抑制其调控的下游基因转录活性,进而抑制脂肪细胞分化(Yu et al.2005)。脂肪细胞特异性敲除NCOR1基因小鼠(AKO小鼠)中PPARγ相关基因上调,而周期素依赖性激酶5 (Cyclin-dependent kinase-5, CDK5)调节的PPARγ ser-273位磷酸化水平下降,而PPARγ磷酸化水平的下降可能进一步激活下游调控因子,促进脂肪形成,导致小鼠肥胖 (Choi et al.2010; Li et al.2011)。而肌肉组织特异性敲除NCOR1基因,导致小鼠肌肉量以及线粒体数量和活性都有所增加,使得小鼠运动耐力增强。进一步研究发现,NCOR1调节了肌肉增强因子2 (Myocyte enhancer factor-2, MEF2)、雌激素受体相关受体(Estrogen receptor related receptor, ERR)和PPARδ等控制肌肉功能的转录因子活性(Yamamoto et al.2011)。上述实验表明,NCoR1作为一个重要的辅抑制子对脂肪细胞分化和肌肉发育有重要作用,使NCoR1作为肥胖病和肌肉萎缩疾病的潜在治疗靶点。同时,NCOR1基因在小鼠上的研究也提示我们该基因可能成为培育产肉量高、肌内脂肪含量高的肉牛新品种的重要候选功能基因。糖皮质激素调控及在成脂分化脂代谢中作用
四丶研究内容 ;
核受体共抑制因子-1(Ncor1)是组蛋白脱乙酰基酶-3(Hdac3)的一个激发因子,是胚胎生成所必需的,但其生理功能却不知道。现在,用缺失Ncor1的基因剔除小鼠所做实验表明,Ncor1-Hdac3相互作用的破坏引起时钟基因的异常调控,导致异常节律行为——睡眠-清醒周期接近23小时,而不是正常的24小时。由于能量消耗增加,这些小鼠还比正常情况下更瘦,对胰岛素更敏感。在活体中,一个功能性Ncor1-Hdac3复合物的失去,会改变几个代谢基因的振荡模式,说明代谢的节律性调控是正常能量平衡的关键。以Ncor1-Hdac3酶为治疗目标,在营养压力型疾病如肥胖症和糖尿病的治疗中,可能是一种具有高度特异性的干预手段。
五丶研究方法及技术路线;
利用病毒敲除了小鼠肌肉中的NcoR1。敲除后,线粒体全力工作,小鼠能够比对照跑得更快更远。转录共调控因子控制了许多转录因子的活性,被认为对基因表达模式有着广泛的影响。在本研究中,敲除了小鼠肌肉中的NcoR1,发现肌肉量以及线粒体数量和活性都有所增加,使得小鼠运动耐力增强。处理过的小鼠在2小时内能跑1600米,而对照小鼠只能跑800米。在小鼠中,NCoR1调节了MEF2、PPARβ/ 和ERR等控制肌肉功能的转录因子活性。NCoR1水平的降低导致这些转录因子的激活,从而促进了氧化代谢。通过敲除NCoR,极大地提高了小鼠的胰岛素敏感性,从而揭示了一种细胞作用新机制,提出了糖尿病治疗的新思路。 研究人员创建了一个基因敲除小鼠模型(AKO),这一模型中脂肪细胞缺乏NCoR,研究人员发现这种模型小鼠即使喂食了易导致肥胖和糖尿病的食物,但是依然存在葡萄糖耐受性,而且这些小鼠还表现出肝脏,肌肉,脂肪中的胰岛素敏感性,以及系统炎症的降低,这些数据都表明一旦敲除NCoR,整个动物体内的胰岛素敏感性大幅度提高了。研究人员发现,在AKO小鼠中,脂肪组织中PPAR 响应基因上调,而CDK5介导的PPAR ser-273磷酸化降低,创建出一个持续激活的PPAR 状态。这表明NcoR作为一个接头蛋白,增强了CDK5的活性,并磷酸化PPAR
六丶预期结果;
NCoR1作为一个重要的辅抑制子对脂肪细胞分化和肌肉发育有重要作用,使NCoR1作为肥胖病和肌肉萎缩疾病的潜在治疗靶点。同时,NCOR1基因在小鼠上的研究也提示我们该基因可能成为培育产肉量高、肌内脂肪含量高的肉牛新品种的重要候选功能基因。糖皮质激素调控及在成脂分化脂代谢中作用
七丶研究的创新点;
NCOR1与NCOR2(NCOR1旁系同源)可以特异结合脂肪细胞分化重要调节蛋白PPARγ,并抑制其调控的下游基因转录活性,进而抑制脂肪细胞分化(Yu et al.2005)。脂肪细胞特异性敲除NCOR1基因小鼠(AKO小鼠)中PPARγ相关基因上调,而周期素依赖性激酶5 (Cyclin-dependent kinase-5, CDK5)调节的PPARγ ser-273位磷酸化水平下降,而PPARγ磷酸化水平的下降可能进一步激活下游调控因子,促进脂肪形成,导致小鼠肥胖 (Choi et al.2010; Li et al.2011)。而肌肉组织特异性敲除NCOR1基因,导致小鼠肌肉量以及线粒体数量和活性都有所增加,使得小鼠运动耐力增强。进一步研究发现,NCOR1调节了肌肉增强因子2 (Myocyte enhancer factor-2, MEF2)、雌激素受体相关受体(Estrogen receptor related receptor, ERR)和PPARδ等控制肌肉功能的转录因子活性(Yamamoto et al.2011)
八丶所需主要仪器设备和试剂及工作条件;
冷冻离心机、冷藏冷冻箱、恒温培养箱、超声波细胞粉碎仪、基因扩增仪、微量加样器、高压灭菌仪、电子天平、全温振荡培养箱、紫外分光光度计、超净工作台、电热鼓风干燥箱、电泳仪、电泳槽、PCR仪、凝胶成像系统、净化装置、消毒设备、数字式酸度计、分析天平. 等